what do you think about Nitrimetri??
several about Nitrimetri..
Titrasi
diazotasi ini sangat sederhana dan sangat berguna untuk menetapkan kadar
senyawa-senyawa antibiotik sulfonamida dan juga senyawa-senyawa anestetika lokal
golongan asam amino benzoat. Metode titrasi diazotasi disebut juga nitrimetri
yakni metode penetapan kadar secara kuantitatif dengan menggunakan larutan baku
NaNO3. Metode ini didasarkan pada reaksi diazotasi yak ni reaksi antara amina
aromatik primer dengan asam nitrit dalam suasana asam membentuk garam
diazonium.
Dalam
nitrimetri, BE suatu senyawa sama dengan BM nya karena 1 mol senyawa bereaksi
dengan 1 mol asam nitrit dan menghasilkan 1 mol garam diazonium. Dengan alasan
ini pula, untuk nitrimetri, konsentrasi larutan baku sering dinyatakan dengan M
( molaritas ) karena molaritasnya sama dengan normalitasnya. Pada titrasi
diazotasi, penentuan titik akhir titrasi dapat menggunakan indikator luar,
indikator dalam dan secara potensiometri.
·
Indikator Luar
Indikator
luar yang digunakan adalah pasta kanji-iodida atau dapat pula menggunakan
kertas kanji-iodida, ketika larutan digoreskan pada pasta/kertas, adanya
kelebihan asam nitrit akan mengoksidasi iodida menjadi iodium dan dengan adanya
kanji/ amilum akan menghasilkan warna biru segera. Indikator kanji-iodida ini
peka terhadap kelebihan 0,05-0,10 ml natrium nitrit dalam 200 ml larutan.
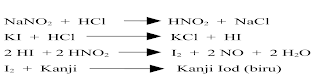
Reaksi yang terjadi dapat dituliskan sbb :
Titik akhir titrasi tercapai apabila pada penggoresan larutan yang dititrasi pada pasta kanji-iodida atau kertas kanji iodida akan terbentuk warna biru sebab warna biru juga terbentuk beberapa saat setelah dibiarkan diudara. Hal ini disebabkan karena oksidasi iodida oleh udara (O2) menurut reaksi :
Untuk
meyakinkan apakah benar-benar sudah terjadi titik akhir titrasi, maka pengujian
seperti diatas dilakukan lagi setelah dua menit. (Ibnu dan Abdul, 2007 :
161-165)
Titrasi
redoks banyak digunakan dalam pemeriksaan kimia karena beebagai zat organik dan
zat anorganik dapat ditentukan dengan cara ini. Namun demikian agar titrasi
redoks ini berhasil dengan baik, maka persyaratan berikut harus dipenuhi :
1. Harus tersedia pasangan sistem
redoks yang sesuai sehingga terjadi pertukaran elektron secara stokhiometri.
2. Reaksi redoks harus berjalan
cukup cepat dan berlangsung secara terukur (kesempurnaan 99%). Harus tersedia
cara penentuan titik akhir yang sesuai. (Rivai, 1995 : 346)
Salah satu
metode yang termasuk dalam titrasi redoks adalah diazotasi (nitritometri).
Titrasi diazotasi berdasarkan pada pembentukan garam diazonium dari gugus amin
aromatis bebas yang direaksikan dengan asam nitrit, dimana asam nitrit ini
diperoleh dengan cara mereaksikan natrium nitrit dengan suatu asam.
Hal-hal yang perlu
diperhatikan pada reaksi diazotasi:
1. Suhu
Titrasi
diazotasi sebaiknya dilakukan pada suhu rendah, lebih kecil dari 15°C karena
asam nitrit yang terbentuk dari reaksi natrium nitrit dengan asam tidak stabil
dan mudah terurai, dan garam diazonium yang terbentuk pada hasil titrasi juga
tidak stabil.
2. Kecepatan reaksi
Reaksi
titrasi amin aromatis pada reaksi diazotasi barjalan agak lambat, titrasi
sebaiknya dilakukan secra perlahan-lahan, dan reaksi diazotasi dapat dikatalisa
dengan penambahan natrium dan kalium bromida sebagai katalisator. (Wunas, 1986
:115)
Sudah kita
lihat bahwa dalam titrasi redoks ada dua jenis indikator, indikator khusus yang
bereaksi dengan salah satu komponen yang bereaksi, dan indikator oksidasi
reduksi yang sebenarnya tidak tergantung dari salah satu zat, tetapi hanya pada
potensial larutan selama titrasi. Pemilihan indikator yang cocok ditentukan
oleh kekuatan oksidasi titran dan titrat, dengan perkataan lain, potensial
titik ekivalen titrasi tersebut. Bila potensial peralihan indikator tergantung
dari pH, maka juga harus diusahakan agar pH tidak berubah selama titrasi
berlangsung. (Harjadi, 1986 : 227)
Dalam titrasi
diazotasi, digunakan dua macam indikator, yaitu indikator dalam dan indikator
luar. Sebagai indikator dalam digunakan campuran indikator tropeolin oo dan
metilen biru, yang mengalami perubahan warna dari ungu menjadi biru kehijauan.
Sedangkan untuk indikator luarnya digunakan kertas kanji iodida . (Wunas, 1986
: 116)
·
Indikator Dalam
Indikator
dalam terdiri atas campuran tropeolin OO dan metilen biru. Tropeolin OO
merupakan indicator asam-basa yang berwarna merah dalam suasana asam dan
berwarna kuning bila dioksidari oleh adanya kelebihan asam nitrit, sedangkan
metilen biru sebagai pengkontras warna sehingga pada titik akhir titrasi akan
terjadi perubahan dari ungu menjadi biru sampai hijau tergantung senyawa yang
dititrasi.
Pemakaian
kedua indicator ini ternyata memiliki kekuarangan. Pada indikator luar harus
dikerahui dulu perkiraan jumlah titran yang diperlukan, sebab kalau tidak tahu
perkiraan jumlah titra yang dibutuhkan, maka sering melakukan pengujian apakah
sudah tercapai titik akhir titrasi atau belum. Di samping itu, kalau sering
melakukan pengujian, dikhawatirkan akan banyak larutan yang dititrasi (sampel)
yang hilang pada saat pengujian titik akhir sementara itu pada pemakaian
indicator dalam walaupun pelaksanaannya mudah tetapi seringkali untuk mengatasi
hal ini, maka digunakan metode pengamatan titik akhir secara potensiomerti.
a. Metode Potensiometri
Metode yang
baik untuk penetapan titik akhir nitrimetri adalah metode potensiometri dengan
menggunakan electrode kolomelplatina yang dicelupkan ke dalam titrat. Pada saat
titik akhir titrasi (adanya kelebihan asam nitrit), akan terjadi depolarisasi
elektoda sehingga akan terjadi perubahan arus yang sangat tajam sekitar +0,80
Volt sampai +0,90 Volt. Metode ini sangat cocok untuk sampel dalam bentuk
sediaan sirup yang berwarna.
Tirtasi
diazotasi dapat digunakan untuk :
a Penetapan kadar senyawa-senyawa yang
mempunyai gugus amin aromatis primer bebas seperti sulfanilamid.
b) Penetapan kadar senyawa-senyawa yang
mana gugus amin aromatic terikat dengan gugus lain seperti suksinil
sulfatiazol, ftalil sulfatiazol dan parasetamol. Pada penetapan kadar senyawa
yang mempunyai gugus aromatic yang terikat dengan gugus lain seperti suksinil
sulfatiazol harus dihidrolisis lebih dahulu sehingga diperoleh gugus amin
aromatis bebas untuk selanjutnya bereaksi dengan natrium nitrit dalam suasana
asam membentuk garam diazonium. Reaksi yang terjadi pada analisis suksinil
sulfatiazol.
c) Senyawa-senyawa yang mempunyai
gugus nitro aromatis seperti kloramfenikol. Senyawa-senyawa nitro aromatis
dapat ditetapkan kadarnya secara nitrimetri setelah direduksi terlebih dahulu
untuk menghasilkan senyawa amin aromatis primer. Kloramfenikol yang mepunyai
gugus nitro aromatis direduksi terlebih dahulu dengan Zn/HCI untuk menghasilkan
senyawa amin aromatis primer yang bebas yang selanjutnya bereaksi dengan asam
nitrit untuk membentuk garam diazonium.
Dalam
farmakope indonesia, titrasi diazotasi digunakan untuk menetapkan kadar adalah
benzokain; primakuin fosfat dan sediaan tabletnya; prokain HCl; sulfasetamid;
sulfametazin; sufadoksin; sulfametoksazol; tetrakain; dan tetakain HCl.
(http//pharmaceutical world.blogspot.com)
Titrasi
nitrimetri merupakan titrasi yang dipergunakan dalam analisa senyawa-senyawa
organik,khususnya untuk persenyawaan amina primer. Penetapan kuantitas zat didasari
oleh reaksi antarafenil amina primer (aromatic) dengan natrium nitrit dalam
suasana asam menbentuk garamdiazonium. Reaksi ini dikenal dengan reaksi
diazotasi, dengan persamaan yang berlangsungdalam dua tahap seperti dibawah ini
:
NaNO2 + HCl → NaCl + HONO
Ar- NH2 +
HONO + HCl → Ar-N2Cl +
H2O
Reaksi ini
tidak stabil dalam suhu kamar, karena garam diazonium yang terbentu
mudahtergedradasi membentuk senyawa fenol dan gas nitrogen. Sehingga reaksi
dilakukan pada suhudibawah 15 oC. Reaksi diazotasi dapat dipercepat
dengan panambahan garam kalium bromida.Reaksi dilakukan dibawah 15 oC,
sebab pada suhu yang lebih tinggi garam diazonium akanterurai menjadi fenol dan
nitrogen.
Reaksi
diazonasi dapat dipercepat dengan menambahkankalium bromida.Titik ekivalensi
atau titik akhir titrasi ditunjukan oleh perubahan warna dari pasta kanji
iodideatau kertas iodida sebagai indicator luar. Kelebihan asam nitrit terjadi
karena senyawa fenilsudah bereaksi seluruhnya, kelebihan ini dapat berekasi dengan
yodida yang ada dalam pastakanji atas kertas, reaksi ini akan mengubah yodida
menjadi iodine diikuti dengan perubahanwarna menjadi biru.
Kejadian ini
dapat ditunjukkan setelah larutan didiamkan selama beberapamenit. Reaksi
perubahan warna yang dijadikan infikator dalam titrasi ini adalah :
KI +HCl → KCl + HI
2 HI + 2 HONO
→ I2 + 2 NO + H2O
I2 + Kanji
yod (biru)
Penetapan
titik akhir dapat juga ditunjukkan dengan campuran tropiolin dan metilen blue
sebagaiindikator dalam larutan. Titik akhir titrasi juga dapat ditentukan
dengan teknik potensiometrimenggunakan platina sebagai indikator elektroda dan
saturated calomel elektroda sebagai elektroda acuan. Pada berbagai macam
indikator yang digunakan dalam titrasi nitrimetri ini, maka dapat dikatakan
bahwa setiap indikator tersebut memiliki keuntungan dan kerugian . salah
satunya adalah indikator luar, dimana keuntungan dari indikator ini adalah
terjadinya perubahan warna yang jelas, sedangkan kerugiannya adalah :
a. Pelaksanaan
tidak praktis karena kita harus menggoreskan setiap kali penambahan titran.
b.
Larutan yang dititer harus didinginkan.
c.
Memerlukan reaksi orientasi untuk memperkirakan titik akhir titrasi.

Tidak ada komentar:
Posting Komentar